Pour bien comprendre le fonctionnement d’un écosystème captif, il est absolument indispensable de connaître quelques notions de chimie des eaux de l’aquarium. Quand vous serez bien familiarisé avec cette chimie un peu particulière, alors je vous recommande la lecture du « Précis technique de l’aquarium marin » de Claude Vast, sûrement le meilleur livre écrit sur le sujet jusqu’à maintenant.
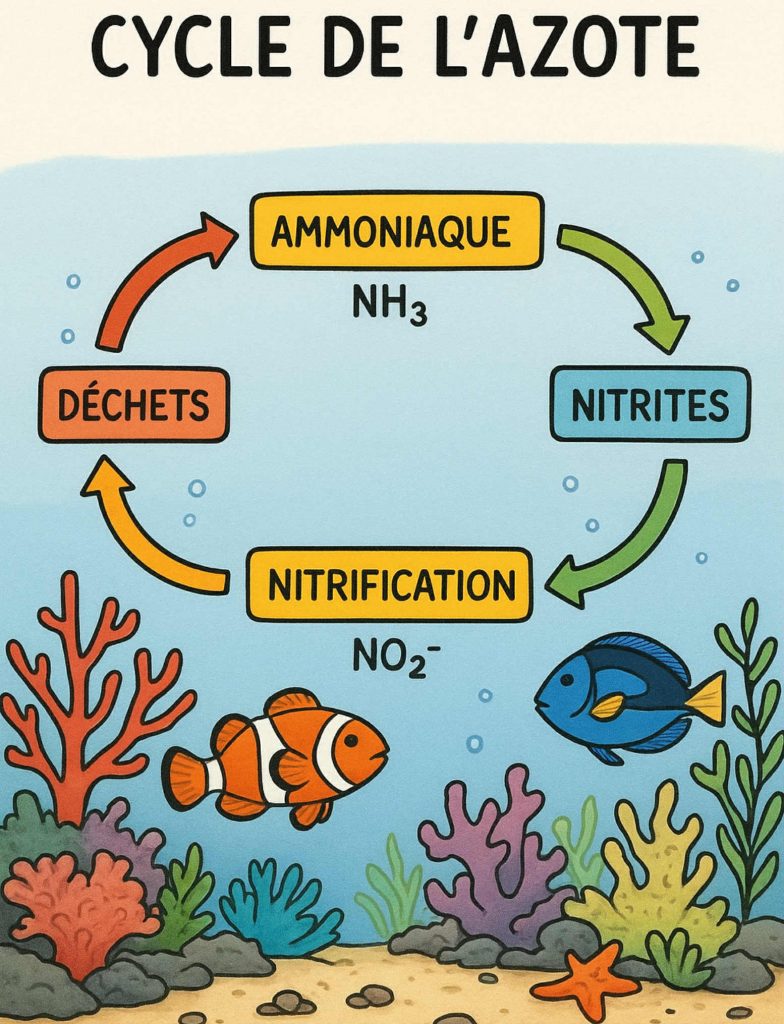
Je pars du principe que maintenant tout aquariophile connait le fameux ‘cycle de l’azote’ .
Un seul maitre mot en récifal : La Stabilité !
Le pH
Le pH, autrement dit le potentiel hydrogène est un élément important en aquariologie marine et récifal. Il est nécessaire de le tester de temps en temps, voir de jeter un œil tous les jours si vous possédez une sonde et son pH mètre.
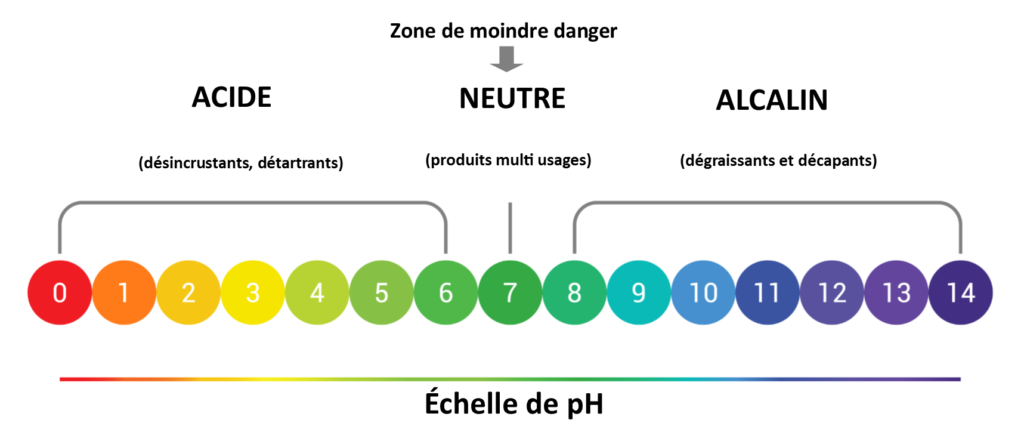
Son importance est maintenant bien connue en aquariologie récifale mais de nos jours, de moins en moins d’aquariophile teste leur eau afin de contrôler la valeur du pH. Pourtant, dans un milieu confiné comme l’aquarium, il est nécessaire de maîtriser tout les paramètres physico-chimiques de l’eau. La valeur du pH conditionne la santé des poissons, des invertébrés, des coraux, et bien plus encore…
Le pH idéal en eau de mer est situé entre 8.2 et 8.4 l’eau de mer est donc une eau alcaline. Plus le pH est bas, plus l’eau est acide. Il est important en récifal d’apprendre à « gérer » son pH, tout au moins de le contrôler un peu.

Il y a toujours, dans un bac qui fonctionne bien, une variation du pH dans la journée. (par exemple 7.8 le matin et 8.4 le soir) Ceci s’explique par le fait que les algues (supérieurs et inférieurs) et les coraux, produisent du gaz carbonique, ce qui engendre une augmentation de l’acidité, donc une diminution du pH. La baisse du pH intervient la nuit, lorsque les algues n’ont plus d’activité photosynthétique. Un peu moins si vous utilisez un réacteur à algues.
Filtrer l’eau du bac à travers du sable de corail ou d’aragonite peut stabiliser le pH, (mais attention à l’accumulation de nitrates dans ce type de système, le débit doit être élevé) comme le réacteur à calcaire (à condition qu’il soit bien réglé), ou l’adjonction d’eau de chaux (le pH en sortie est élevé mais l’adjonction régulière d’eau de chaux tend à maintenir un pH relativement stable, aux alentours de 8.2)
Si vraiment vous avez des problèmes de stabilité du pH dans votre bac et que le taux reste constamment en dessous de 8, il existe une résine en forme de granulés absorbants qui se place sur l’arrivée d’air de votre écumeur, les granulé se mettent dans un petit réacteur, à placer dans la partie sèche de votre décantation. (fauna marin) Ce système peu utilisé est à même de renforcer l ‘efficacité de votre écumeur…
L’adjonction d’eau de chaux fera aussi monter le taux de calcium, idéal pour les coraux durs, les invertébrés, les bénitiers, et dans une moindre mesure, les coraux mous. Il est à noter qu’en milieu naturel, il n’y a pas ou très peu de variations de l’équilibre acido-basique, c’est ce qui rend nos aquariums différents et plus difficile à gérer. Si vous possédez un pH mètre à sonde, pensez à l’étalonner de temps en temps selon les recommandations du fabricant.
2 solutions pour tester votre pH. Le bon vieux test chimique colorimétrique, (peu fiable mais économique) ou bien le pH-mètre électronique; Ne parlons pas des tests en bandelettes qui ne sont pas très fiables en aquariophilie marine bien qu’elles peuvent vous donner une simple indication.
Un bon brassage en surface du bac augment les échanges gazeux entre l’air et l’eau et aide à maintenir un bon pH.(à condition que votre pièce soit aérée régulièrement)
Il est très rare qu’il faille baisser manuellement le taux de pH en marin, contrairement aux aquariums à Discus par exemple qui se plaisent dans un pH de 6 ! Mais en cas d’extrême urgence pensez au dioxyde de carbone ou au bicarbonate de soude.
Le TH
Le TH (titre hydrotimétrique) ou le GH (valeur allemande) représente le taux des ions calcium et de magnésium. Cette valeur est exprimée en degré. Cette unité est usuel en eau douce. Le th français correspond à 10 mg CaCO3 par litre. 1 th = 0.56 gh allemand. C’est en fait la valeur de la dureté de l’eau.
L’ eau de mer a un titre hydrotimétrique d’environ 750 degrés français. (wiki)
Le TAC
Le tac (titre alcalimétrique complet) représente la concentration en bicarbonate (hydrogénocarbonate) et en carbonate(calcium et magnésium). Cette valeur est aussi exprimée en degré. Le tac se nomme » la dureté carbonatée » : KH en allemand. Le KH en eau de mer doit être entre 7 et 12 degrés. 1 degré allemand = 1.78 degrés français.
Pour remonter le TAC en eau de mer, on utilise de « l’eau de chaux ».(ajouté de préférence en goutte à goutte sur une sortie de pompe de brassage ou aux mieux dans la décante, surtout mettre uniquement l’eau claire et non pas la solution blanchâtre(le lait de chaux !) qui elle reste au fond de votre récipient.
Le GH et le KH se mesurent en degrés allemands car la plupart des test colorimétriques vendus dans le commerce aquariophile proviennent d’Allemagne.
Le rH
Le rH est appelé potentiel redox ou potentiel d’oxydoréduction. C’est la mesure de l’action oxydante de l’eau. Une oxydation trop puissante ou trop basse peut être la cause et la source de nombreux problèmes. (taux d’oxygène réduit, brûlures des branchies, asphyxies des poissons, productions de gaz néfastes, etc..)
Le potentiel redox est dépendant de la température et il est lié à la valeur pH de l’eau. En contrôlant le rH sur une certaine période (permanente de préférence) nous pouvons voir si les conditions physicochimique de l’aquarium sont stables et aussi connaître le pouvoir de recyclage du bac. Un aquarium marin en bonne santé doit avoir une valeur redox comprise entre 350 mV et 450 mV. On ne croise plus beaucoup de récifaliste qui teste leur rH.
Les Nitrites
Les nitrites sont dangereux pour tous les occupants de l ‘aquarium. Le taux doit être contrôlé régulièrement surtout lors de la phase de démarrage. Un taux important survient en général lors de la mise en route du bac ou lorsque l’eau est surchargée en matières organiques et que les bactéries ne sont pas suffisantes pour les transformer en nitrates. A noter que les américains eux contrôlent le taux d’ammoniac.
Cela arrive aussi parfois lorsque vous rajoutez de nouvelles pierres vivantes, c’est la raison pour laquelle il est conseillé de mettre les pierres vivantes en une seule fois, et de surtout bien les « nettoyer » à l’eau de mer, brossage léger et rinçage.
En cas de montée de nitrites, vous devez donc réensemencer votre bac artificiellement afin de faire baisser le taux de nitrites.(Bactéries Tunze, par exemple ou biodigest de prodibio) Éventuellement un changement d’eau important (au moins 30% ) pourra vous y aider.
Les Nitrates
Contrairement aux nitrites, les nitrates (NO3) sont moins dangereux pour les organismes marins. Mais attention, les invertébrés n’aiment en général pas du tout les nitrates, alors il est préférable de contrôler régulièrement ce taux. Un bac sain n’en contient qu’une quantité à peine mesurable. Un bac remplie de Lps peut supporter un taux un peu plus important, contrairement à un bac de Sps.
Dans la plupart des cas, il vaut mieux avoir une teneur en nitrates inférieur à 10 mg/l. Les coraux durs sont plus sensibles aux nitrates et leur croissance peut stopper voir régresser. Le mieux est d’introduire des algues supérieures comme des caulerpes ou de la chaeto, qui sont de véritables pompes à nitrates, si vous ne pouvez pas les introduire dans le bac principale, pensez à faire un refuge dans votre décante. ou le mieux un réacteur à algues. Avec un taux de nitrates trop élevé, vous risquez aussi de favoriser le développement des algues indésirables.
Un taux de nitrates élevé est moins dangereux que les nitrites pour nos poissons, mais avec un empoisonnement progressif, régulier et sur le long terme vous avez un risque de pathologies diverses comme une difficulté respiratoire ou encore une perte d’équilibre (un peu comme le problème de vessie natatoire) ou encore une perte d’appétit pouvant aller jusqu’à la mort de l’individu.
La quadrature du cercle pour les récifalistes et le taux de nitrates/phosphates, le pH et le KH, si ces paramètres sont stables dans le temps, les autres paramètres suivront et votre bac deviendra équilibré et viable sur le long terme.
Il existe aussi une technique de filtration sur souffre qui diminue la teneur en nitrates.(technique mise au point entre autre par Mr Marc LANGOUET) Il faut 1 % du volume du bac en billes de souffre. Le pH à la sortie étant relativement faible, il faut absolument faire passer l’eau sur un substrat calcaire afin de remonter le pH à des valeurs un peu plus acceptable pour un bac récifal. Vous pouvez retrouvez son article sur cette page.
L'ammoniac

L’ ammoniac est un élément extrêmement toxique pour nos pensionnaires, en général on ne mesure pas le taux d’ammoniac sauf dans les cas extrêmes, un taux d’ammoniac élevé peut provenir suite à la mort d’un poisson ou d’un invertébré et à la décomposition de son cadavre dans le bac.
Il est bon de savoir que l’ammoniac est encore plus toxique si le pH est élevé. La valeur dans l’aquarium ne doit jamais dépasser 0,1 ppm. L’eau de transport des poissons tropicaux est naturellement chargée en ammoniac, la cause est, entre autre, les fèces du poisson durant le voyage.
L’ammoniac est un gaz mortel pour l’humain à très haute dose, mais rassurez vous, le cycle de l’azote est là justement pour éliminer l’ammoniac et le transformer en nitrites puis en nitrates. Si vous avez un soucis de cet ordre, recherchez le cadavre dans l’aquarium ou la cause de cette pollution afin de l’extraire et effectuez un changement d’eau d’au moins 30%.
Les phosphates
Les phosphates (PO4) se concentrent dans l’aquarium par la nourriture distribuée aux poissons et aux coraux mais aussi par l’eau de rajout si celle-ci n’est pas osmosée. Un taux de phosphates important peut être une source d’envahissement par les algues inférieurs. De plus, les phosphates peuvent bloquer la croissance des coraux et baisser leur coloration car ils absorbent le calcium indispensable à la formation du squelette corallien. Il faut aussi faire très attention à certains sels synthétiques de qualité médiocre, même chose pour le sable coralien.
Si vous avez ce type de problème avec vos coraux, pensez donc à contrôler votre taux de phosphates. L’idéal est de tourner autour de 0,02 Mg/l. Les phosphates organiques sont normalement éliminés par l’action de l’écumeur si celui ci est bien dimensionné, bien entretenu et bien réglé.
Un nourrissage parcimonieux, l’ introduction de détritivores divers, d’escargots et le rajout d’un matériau filtrant spécial anti phosphates (oxyde de fer) peuvent vous aider à rétablir un équilibre dans le bac. ( l’oxyde d’aluminium, marche parait il très bien, en très faible quantité, pourtant, il est semble t-il, inefficace à partir d’un PH de 7.5 ! )
Un taux de phosphates élevé peut conduire à l’eutrophisation de votre bac et une arrivée d’algues inférieurs et de diatomées. C’est en général là, que les ennuis commencent…Il est peut être temps d’effectuer un bon changement d’eau si vous ne pratiquez pas cette technique régulièrement.
L’ajout d’eau de chaux peut contribuer à lutter contre les phosphates. (l’eau de chaux précipite les phosphates dissous dans l’eau et transforme ceux-ci en matière insoluble sous forme solide non assimilable) Si votre bac est filtré avec du charbon actif, vérifiez bien que celui ci est sans phosphates, les charbons de mauvaises qualités en contiennent.
Il est à noter que le phosphore (la transformation de matières organiques dispense du phosphore sous forme de phosphates) est une substance importante pour la pousse des algues. (inférieurs et supérieurs)
Le filtre à algues ou encore un réacteur à algues sont aussi des alliés contre un taux de phosphates trop élevé, mais attention en cas de Lyse des algues vous pouvez vous retrouver avec une augmentation de votre taux de PO4. Ne pas oublier aussi que le surpeuplement du bac peut être aussi la cause du déséquilibre. Vous trouverez dans le commerce des tas de résine anti phosphates mais le plus important est de réfléchir à la cause de cette augmentation dans votre bac.
Le Silicium
L’apparition dans nos aquariums d’algues brunes, de cyanobacteries ou de diatomées est souvent due à un taux élevé de silicium (mis à part un éclairage défectueux ou inadéquate ou bien encore un encrassement de l’écumeur), vous pouvez lutter contre cela en utilisant uniquement de l’eau osmosée lors de vos changements d’eau ou lors de vos rajouts d’eau évaporée, car l’eau du robinet est souvent trop riche en acide silicique.
Si ces algues disparaissent, c’est parce qu’elles ont tout simplement épuisées tout le silicium disponible dans le bac.(la valeur des silicates ne doit pas dépasser 0.2 mg/l) Ne pensez donc pas remédier au problème en effectuant un changement partiel de votre eau car dans ce cas ce sont les algues elles même que vous allez nourrir !
Attention aussi aux eaux en bouteille, préférez toujours l’eau osmosée.
Attention aussi à votre substrat, si il est de mauvaise qualité, il se peut qu’ il ait une très forte concentration en silicium. Il existe maintenant des tests pour tester le taux de silicium dans votre bac.

Le calcium

Le calcium (Ca) est indispensable à la construction du squelette corallien. Il est présent dans l’eau de mer sous forme dissoute, et il est partiellement absorbé par les coraux (puis synthétisé) mais aussi par les mollusques (pour leur coquille, leur carapace). La synthèse de ce carbonate de calcium à besoin de 2 éléments : le dioxyde de carbone et le calcium sous forme ionique.
La solubilité du carbonate de calcium dépend de la température, de la pression et de la salinité de l’eau. La concentration en calcium diminue progressivement dans le bac car les organismes l’absorbent et le consomment, il faut donc procéder à un apport constant en calcium. Il y a plusieurs procédés pour cela :
l’eau de chaux (hydroxyde de calcium)
le réacteur à calcium (automatisation de l’apport d’eau de chaux)
la supplémentation par apport de calcium liquide
les changements d’eau réguliers à hauteur de 10 % du volume du bac, voir 20 %
Certains sont aussi tentés de pousser le taux de calcium au delà de 600 mg/l. Encore une fois, mieux vaut rester dans des valeurs approchant le taux naturel, les résultats ne sont jamais à la hauteur de nos espérances. Un certain chinois dans les années 60 avait déjà tout compris… Le taux naturel du calcium dans l’eau de mer est d’environ 420 mg/l (taux qui me semble un bon compromis en bac mixte) ne dépassez pas 500 mg/l.
Dans le cadre d’un apport en calcium liquide je vous recommande les produits suivants :
Reef calcium de seachem
Calcium pro de Grotech
Carbo calcium et components calcium de Tropic marin
Calcium ATI
CA + de Aquaforest
Calcium X pro de Aquatic nature
Microbe lift calcium
Aquarium systems reef shot calcium
Calcium + de colombo
Dupla calcium
Le magnésium

C’est un composant extrêmement important en eau de mer, d’ailleurs, le troisième en quantité après le chlorure et le sodium (qui en s’associant forment le chlorure de sodium) car la teneur du Mg en eau de mer naturelle est d’environ 1300 mg/l. (quand le calcium reste lui à 410 mg/l !) Le calcium s’évapore (façon de parler) rapidement si la teneur en magnésium baisse, l’un ne va pas sans l’autre…
Le magnésium (Mg) est aussi un élément important dans la croissance des algues corallines. Une récente découverte nous démontre que le magnésium aide à lutter contre les phosphates (la liaison du phosphate n’est possible qu’avec un taux suffisant de magnésium dans le bac.)
La supplémentation dans un bac récifal ne saurait se passer sans magnésium quelque soit la méthode. Pour ma part il m’arrive de pratiquer de temps en temps et en quantité raisonnable un apport de magnésium dans mes bacs avec une solution de la marque Preis.
Le problème principal est que l’adjonction d’hydroxyde de calcium régulière peut provoquer une forte carence en magnésium, car il peut y avoir une précipitation des sels de magnésium sous une forme insoluble. Il faut donc dissocier et espacer ces deux apports dans le temps.
La norme est de 1,30 g/l. Dans les bacs qui présentent une carence en magnésium, le calcium s’épuise plus rapidement que le carbonate de calcium, il est donc important de ne pas négliger cet apport dans les aquariums contenant de nombreux coraux durs (sps/lps) et/ou mous…
Evidement la consommation du magnésium est variable en fonction de la biomasse de votre aquarium.

L'Eau Osmosée

On en parle beaucoup, et ce n’est pas pour rien… L’eau osmosée est la résultante d’une technique appelée : l’osmose inverse. L’eau de nos villes et même de nombreuses campagnes est vraiment polluée, elle est bien sur consommable par les humains (quoique…!), mais dans le cas qui nous intéresse, mieux vaut avoir une qualité d’eau irréprochable afin d’éviter les futurs problèmes. C’est la raison pour laquelle nous faisons appel à cette technique maintenant parfaitement maîtrisée depuis plusieurs années et qui nécessite un investissement assez léger.
L’eau qui circule dans nos canalisations est soumise à une certaine pression, c’est donc cette pression que nous allons utilisée pour introduire l’ eau de conduite dans l’appareil. Cette eau passera d’abord dans un préfiltre afin de retirer entre autre, le chlore, puis elle passe ensuite dans une membrane (sensible au chlore) qui retire tout les sels minéraux, toutes les impuretés, les oligo-éléments, les dioxines, les pesticides, les herbicides, les métaux lourds, (mercure, zinc, plomb, cuivre) les bactéries, les virus, les nitrates (normalement) et tout le reste.
Conclusion, vous avez de l’eau pure à 98 % qui sort du système. Idéal pour l’aquariophilie récifale ou marine. Le seul reproche que l’on peut faire à ce système est la consommation excessive d’eau, en effet, il faut 4 litres d’eau de rejet pour 1 litre d’eau osmosée.(en moyenne, pour les osmoseurs haut de gamme c’est 1 pour 1) (comptez 750 euros pour un modèle haut de gamme, 120 euros pour un bon modèle, environ 49 euros pour un modèle bas de gamme sur le net)
A chaque fois que vous ouvrez votre osmoseur, jetez au moins les 5 premiers litres.
Le Gaz Carbonique
Une mode se profile à l’horizon, qui est de rajouter du gaz carbonique dans les bacs marins ! On croit rêver ?! (pratique souvent utilisée en eau douce et dans les bacs abondamment plantés) Sous prétexte que certains anthozoaires absorbent du CO2 en grande quantité, on surdose l’eau en faisant des injections contrôlées, le résultat est sans appel : une forte poussée d’algues filamenteuses…D’autre part, faut-il rappeler que l’air que nous respirons contient déjà du gaz carbonique ? L’échange se fait donc en surface de nos bacs, et ce, en quantité suffisante. D’ailleurs, j’en profite pour vous rappeler qu’il est absolument nécessaire dans un bac marin de bien brasser la surface de l’eau, même énergiquement. Ce qui est applicable en eau douce ne l’est pas forcement en eau de mer. L’injection du CO2 dans un bac marin peut éventuellement se faire avec un réacteur à calcaire à injection (et avec l’aide d’un Ph mètre électronique pour vérifier le taux de Ph)afin de dissoudre des granulés calcaires qui sont sensés maintenir un taux de calcium élevé et maintenir un Kh à 8, mais jamais directement dans le bac.


Le Strontium
Le strontium est un élément primordial pour le bac récifal, il participe à la calcification du squelette des coraux en le renforçant, le solidifiant et au renforcement de leur système immunitaire (tout comme les vitamines et acides aminés)
Vous pouvez contrôler le taux de strontium dans le bac avec un test ICP, la valeur doit tourner autour de 8 mg/l. Si vous avez un déficit de strontium vous pouvez ajouter du reef shot strontium de aquarium system, pratique car pas de risque de surdosage. (fiole de 20 mg/l pour 200 litres)
A noter que le strontium est aussi bénéfique aux invertébrés tes les escargots, les bénitiers et autres bivalves, les bernard, les crevettes, et la coralline.
Attention au surdosage et vérifier votre sel, certains on un taux assez élevé en strontium parfois jusqu’à 12 mg/l, il ne faut pas dépasser 15 mg/l.
Test Icp
Un test Icp est un test global de votre eau et parfois de votre eau osmosée. (Attention aux surprises ! ) Ces tests sont assez chers (de 20 à 50 euros) mais utiles une ou deux fois par an, tous les mois si vous en avez les moyens…
On trouve dans le commerce des box icp comme ATI ou Fauna Marin ou Aquaforest.
La technologie ICP-AES est une bonne technique d’analyse pour mesurer la nature et la concentration des éléments qui se trouvent dans les matières solides, les liquides ou les gaz. ICP-AES est l’acronyme de Inductively Coupled Plasma – Atomic Emission Spectrometry (Plasma à couplage inductif – Spectrométrie d’émission atomique). De par sa grande précision (ppb – parties par milliard), la technologie ICP-AES convient parfaitement à l’analyse des oligo-éléments, c’est-à-dire les éléments à très faible concentration.

Par exemple le test Marinlab :
Analyse d’eau en laboratoire de MarinLabs utilisant la technologie ICP-OES. Ce kit permet une analyse de l’eau de votre aquarium.
Analyse de 36 éléments : Li, Si, I, Ba, Mo, Ni, Mn, Be, Cr, Co, Fe, V, Zn, Hg, Se, Cd, Sn, Sb, As, Al, PB, Ti , Cu, La, Sc, W, Na, Ca, Mg, K, Br, B, Sr, S, P, PO4 + Salinité + KH
En général vous remplissez 2 ou 3 fioles de votre eau, puis envoi par la poste et vous recevez les résultats complets par mail avec les recommandations si votre eau pose problème.
Centrale de tests pour particulier
Pour les véritables passionnés récifalistes, le graal ultime !

Alkatronic est un produit tout-en-un destiné aux amateurs de récifs sérieux pour surveiller et stabiliser automatiquement l’alcalinité de votre système récifal. Le produit fonctionne dès la sortie de la boîte sans avoir besoin d’aucun autre équipement. Ce produit a été conçu à l’origine par Jonas Roman de Suède et est commercialisé avec FOCUSTRONIC.
Maintient et contrôle le dKH en dessous ou au-dessus des niveaux souhaités.
La Rolls des appareil de mesure automatique est en ce moment, « le Mastertronic » capable de mesurer les PO4/NO3/Ca/Mg/dKH*/OLI et d’autres paramètres, comptez 1500 euros.

PO4: 0.01 ppm / 0.005 ppm
Mg: 20 ppm / 20 ppm
Ca: 6 ppm / 6 ppm
dKH: 0.1 dKH / 0.05 dKH
L'eau de mer naturelle

Si vous tenez absolument a mettre de l’eau de mer naturelle, il est évident pour tout le monde qu’il faille la puiser assez loin du rivage, surtout en France malheureusement. La pollution sur nos côtes est encore trop importante. Allez au moins à 300 mètres des côtes, et prenez l’eau en profondeur et non en surface. Si vous pouvez directement la filtrée avec micron bag, (pas en dessous de 300 micron) c’est encore mieux. Il faut la brasser énergiquement et l’oxygéner avant de la mettre dans votre bac.(ne pas oubliez d’équilibrer la densité avec de l’eau osmosée si elle est trop importante)
Attention, plus la température augmente, plus la densité baisse. Si possible, l’eau doit être stockée à l’abri de toute source lumineuse afin d’éviter une prolifération de bactéries. Vérifiez aussi la température. Il est inutile de la filtrer encore une fois (comme j’ai pu souvent le lire) car vous perdriez tout le bénéfice du micro/macro plancton contenu dans l’eau. Ensuite, versez là au goutte à goutte à température équivalente dans votre bac en ayant pris soin de contrôler le taux de nitrates, de nitrites et de phosphates.(tout doit être normalement à 0 mg/l) Tout ça c’est bien joli, mais moi j’habite loin de la mer et je n’ai pas de bateau, alors ?
Certains commerces vendent de l’eau de mer naturelle, mais je ne vous le conseille pas, il vaut mieux l’avoir « fraîche ». Elle est en général stockée trop longtemps chez le détaillant et vous en perdriez tout son bénéfice. Mais vous pouvez essayer aussi les aquariums publics (près des côtes), parfois ça marche…
Aquavie (Osmopur Marine) vends de l’eau de mer synthétique stérilisée , parfait pour un nano récif ! Une corvée de moins, si vous avez moins de 60 litres…

Notice du « fabricant » : L’eau osmosée OSMOPUR MARINE est un mélange d’eau osmosée de très haute qualité (0,01ms), émulsionnée avec le nouveau sel provenant du laboratoire américain de réputation mondiale SEACHEM (Vibrant Sea), le tout traité ensuite par ultraviolet avant son conditionnement. OSMOPUR MARINE est une eau de mer prête à l’emploi pour aquarium. Caractéristiques : Densité 1023 à 25°C -Calcium (Ca) 425-445 mg/L – Potassium (K) 500-550mg/L – dKH 8-9.5° – pH 8.2-8.5 – Magnésium (Mg) 1256-1350 mg/L et Strontium 8-10 mg/L.
Pour stocker l’eau chez vous, utilisez des bidons en plastique de qualité alimentaire ou bien des cuves en verre collé, il faut absolument la brasser énergiquement en surface et en profondeur, la chauffer à 25 degrés et ne surtout pas dépasser une semaine de stockage. Vous verrez que l’eau de mer naturelle a un effet bénéfique sur les tous animaux de l’aquarium. Faites-le l’hiver car la pollution est moins importante qu’en été.( je ne dis pas ça pour les crèmes solaires !) Il faut reconnaître que cette technique ne concerne que quelques amateurs privilégiés…Pour le reste des récifalistes, le sel synthétique fera parfaitement l’affaire. Ci dessous de l’eau toute prête : coralseawater de Oceanlife (marque italienne)
La Composition Chimique de l'eau de mer
Il est évident que l’eau de mer synthétique n’a pas les mêmes qualités que l’eau de mer naturelle. Cependant , les industriels ont fait d’énormes progrès et on peut depuis de longues années maintenir dans de parfaites conditions des animaux marins avec de tel sels.
La qualité principale de l’eau de mer naturelle tient au fait qu’elle est chimiquement beaucoup plus complète et « vivante ». A cela on peut répondre que l’eau synthétique possède l’avantage de ne contenir aucun organisme pathogène. Chez les professionnels, revendeurs ou grossistes, les batteries tournent avec des sels synthétiques, dans les aquariums publics, pour la plupart les bacs tournent en eau naturelle pris au large et bien sur traitée, filtrée et sous ultra-violet de type industriel, exception faites des aquariums publics loin des cotes.
Le sel dissous le plus représenté dans l’eau de mer est le chlorure de sodium, d’ailleurs, on défini la salinité en fonction de sa concentration. La norme de définition est exprimée en grammes par litre, la moyenne étant de 35 g/l.
Sachez que l’on retrouve dans l’eau de mer (d’après des analyses extrêmement poussées) quasiment tous les éléments présents sur notre planète. L’eau de mer constitue donc un mélange d’une grande complexité. Voici donc quelques constituants, à nous de définir à quoi ils peuvent servir en biologie marine et particulièrement en aquariophilie récifale :
Principaux composants :
Chlore / Sodium / Magnésium / Calcium / Strontium / Potassium / Soufre / Carbone / Brome / Bore
Autres composants :
Argent / Aluminium / Antimoine / Argon / Arsenic / Barium / Béryllium / Bismuth / Cadmium / Carbonates / Cérium / Cobalt / Cuivre / Chrome / Césium / Crypton / Erbium / Etain / Dysprosium / Europium / Fer / Fluor / Gadolinium / Gallium / Germanium / Hélium / Hafnium Holmium / Indium / Indium / Iode / Lanthane / Lithium / Lutetium / Manganèse / Mercure / Molybdène / Néodyme / Niobium / Nickel / Or / Phosphore / Platine / Plomb / Praséodyme / Protactinium / Radium / Rubidium / Radon / Radium / Samarium / Scandium / Sélénium / Silicium / Tantale / Terbium / Thallium / Thulium / Titane / Thorium / Tungstène / Uranium / Vanadium / Ytterbium / Yttrium / Zinc / Zirconium
Gaz :
Hydrogène / Oxygène / Anhydride carbonique / Argon / Krypton / Néon / Xénon
Éléments en quantité infinitésimales :
Actinium / Astate / Iridium / Francium / Osmium / Platine / Palladium / Rhodium / Ruthénium / Technétium
Ceci étant dit, on a quand même une petite idée de la fonction de certains éléments, d’après S.Fournier et N.Leclercq (deux très bon spécialistes !):
le cobalt à un rôle structurel tout comme le calcium et le strontium, le brome un rôle immunitaire, le chlore à un rôle dans la photosynthèse ainsi que le fer, le potassium agit sur la régulation osmotique, le manganèse sur la structure des coraux et aussi sur la photosynthèse, l’iode sur le métabolisme (et je rajouterai sur la coloration de certains coraux), le sodium sur une activation enzymatique ainsi que le soufre, le molybdène sur une réduction des nitrates et sur la fixation de l’azote atmosphérique et enfin le magnésium sur l’activation enzymatique, la pigmentation photosynthétique (et je rajouterai sur la fixation du calcium ) et le fluor sur la calcification, etc,etc…